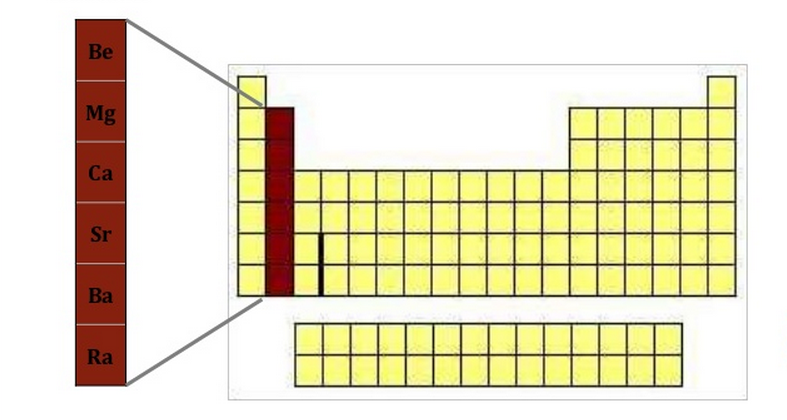
Los metales alcalino-térreos son un grupo de elementos que se encuentran situados en el grupo IIA de la tabla periódica y son los siguientes: berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra). El radio no siempre se considera, pues tiene un tiempo de vida media corta.
El nombre "alcalino-térreos" proviene del nombre que recibían sus óxidos, "tierras", que tienen propiedades básicas (alcalinas).
Metales alcalino-térreos
Esta página fue creada por alumnos de tercer año del liceo Kennedy con el propósito de compartir información acerca de los metales alcalino-térreos. Esperamos que disfruten! Felipe Osorio, Timoteo Casas, Piero Marino y Felipe Mella.
Características
- Tienen dos electrones de valencia.
- Los metales alcalino-térreos son más duros que los metales alcalinos.
- Tienen brillo y color blanco plateado.
- Son más densos que los metales del grupo IA y que el agua.
- Son buenos conductores eléctricos.
- Son muy reactivos pero menos que los alcalinos. Aun así en la naturaleza se encuentran formando sustancias compuestas.
- Forman compuestos iónicos
- Son buenos agentes reductores.
- Los átomos de estos elementos tienden a perder los dos electrones de valencia y se transforman en cationes con doble carga positiva.
Ejemplo:
Ca2+
Ejemplo:
Ca2+
Los dos elementos más importantes de este grupo
Los elementos más importantes de este grupo son el magnesio (Mg) y el calcio (Ca).
Magnesio
Relacionado a la vida, el Mg forma parte de cada molécula de clorofila que hace posible la fotosíntesis en las plantas. Su número atómico es 12 y es el séptimo elemento más abundante del planeta. Fue descubierto por Joseph Black en Grecia en el año 1755.Calcio
El Ca es el quinto elemento más abundante en la corteza terrestre. Forma compuestos que dan rigidez a los caparazones y huesos y también a algunas edificaciones. Su número atómico es 20 y es el quinto elemento que más abunda en nuestro planeta. Lo descubrió Humphry Davy en 1808 en Inglaterra.Detalles de los demás metales alcalinotérreos
Berilio
El berilio (Be) es un elemento tóxico, de color gris, duro, ligero y quebradizo. Su número atómico es 4. Se emplea principalmente como endurecedor en aleaciones, especialmente de cobre. Fue descubierto por Louis Nicolas Vauquelin en el año 1798 en Francia.Estroncio
El estroncio (Sr) es de color plateado brillante. Se oxida rápidamente en presencia de aire y adquiere un tono amarillento por la formación de óxido, por eso debe ser conservado sumergido en parafina. Su número atómico es 38. Hoy en día el principal uso del estroncio es en cristales para tubos de rayos catódicos de televisiones en color, ya que filtran los rayos X evitando que incidan sobre el espectador. También es utilizado para pirotecnia. Fue descubierto en el año 1790 en Escocia por Adair Crawford.Bario
El bario (Ba) es el 18º elemento más común, ocupa una parte de 2.000 de la corteza terrestre. Su número atómico es 56. Es similar al calcio, pero más reactivo. Este metal se oxida con mucha facilidad cuando se expone al aire y es altamente reactivo con el agua o el alcohol. El bario se usa para la pirotecnia, como muchos otros elementos de los grupos A. Su descubridor fue Humphry Davy en Inglaterra en el 1808.Radio
El radio (Ra) es sumamente radioactivo. Es de color blanco, pero se ennegrece con el contacto con el aire ya que se oxida rápidamente. Es el más pesado de todos los metales alcalinotérreos. Su número atómico es 88. Por su gran radioactividad, el radio no tiene muchas utilidades, pero el cloruro de radio se utiliza para producir radón, que es utilizado para tratamientos contra el cáncer. Fue descubierto en el año 1898 por el matrimonio Curie, Marie Curie y Pierre Curie en la República Checa.
Suscribirse a:
Comentarios (Atom)